-
액체생검(Liquid Biopsy)과학(Science)/산업 (Industry) 2023. 6. 12. 23:40
0. 목차
- '액체생검'이란 무엇인가?
- 순환종양세포(CTC)
- 순환종양핵산(cfDNA)
- 엑소좀(Exosome)
- '액체생검'을 통해 '정밀의료'가 가능해진다.
- '액체생검' 관련 기업

1. '액체생검'이란 무엇인가?
기존의 진단 표준방법으로 사용되고 있는 '조직생검(Tissue Biopsy)'은 내시경이나 바늘 등의 도구를 이용하여 환자로부터 침습적인 방법으로 획득한 조직을 분석하는 방법이다. 그러나 '조직생검'은 필수적으로 환자의 고통을 동반하고 위험부담을 가지고 있으며, '발생 부위', '크기', '환자 상태' 등의 요인에 따라 불가능한 경우도 존재한다. 특히 암의 경우 '유전적 이질성(Genetic Heterogeneity)'의 특성이 있어 국소적 부위에서 획득한 조직에 대한 결과로는 부정확한 정보를 제공할 가능성이 있고, 효과적인 치료를 못할 가능성도 존재한다. 이러한 조직생검의 한계를 극복하기 위하여 연구자들은 새로운 진단 방법을 고안하기 위해 다양한 연구를 시도하였고 현재 '액체생검(Liquid Biopsy)'이라는 진단 기술로 패러다임이 바뀌고 있다.
'액체생검(Liquid Biopsy)'은 비침습적 방법으로 '혈액', '침', '소변' 등 환자의 체액을 수집하여 분석하는 방법으로, 조직생검에 비해 환자에게 고통과 위험부담이 현저히 감소될 수 있다. 이러한 액체생검은 2015년 MIT가 발표한 10대 미래 유망기술로 선정되었으며, 2020년 대한민국 생명공학 정책 연구센터에서 10대 바이오 미래 유망기술로 선정되는 등 매우 혁신적인 기술로 여겨지고 있다.
1-1. 액체생검'에 활용될 수 있는 요소
'액체생검'에 활용될 수 있는 요소는 체내에 포함하고 있는 '혈액', '소변', '침', '눈물', '모유' 등 다양한 성분들이다. 현재 연구자 대부분은 해당 성분들을 활용하여 진단 방법을 개발하고 있으며, 대표적인 요소는 '순환종양세포(CTC: Circulating Tumor Cell)', '순환종양핵산(cfDNA, circulating free DNA)', '엑소좀(Exosome)'이 있다. 다만 2023년 현재, 액체 생검의 3가지 주요 요소들을 활용한 기술개발 시도 및 연구가 진행되고 있으나, 다양한 기술적 한계 및 표준화 방법의 부재로 상용화 단계로 쉽게 접어들지는 못하고 있다.
액체생검에 활용되는 대표 요소 설명 순환종양세포(CTC) 악성종양 환자의 말초혈액에서 발견되는 종양세포 순환종양핵산(cfDNA) 암환자의 종양으로부터 방출된 Cell free DNA 엑소좀(Exosome) 모든 살아있는 세포에서 발견되는 '미세소포(Microvesicle)' 2. 순환종양세포(CTC)
악성종양 환자의 말초 혈액에서 발견되는 종양세포를 '순환종양세포(CTC: Circulating Tumor Cell)'라고 하며, 원발 종양 및 전이가 진행된 조직으로부터도 유래된다고 알려져 있다.
'순환종양세포(CTC)'를 활용한 암 진단 시도에는 '세포 분리', '샘플 조제', '샘플 분석'을 위한 다양한 최신 기술들이 적용되고 있다. 현재까지는 주로 안정적으로 '순환종양세포(CTC)'를 분리하기 위한 '분리회수율·분리순도 증가', '재현성 향상', '분리의 자동화'를 중심으로 기술 개발이 집중되었다. '샘플 조제' 단계에는 microfluidics, whole genome amplification 기법 등 다양한 기술들이 활용되어 연구되고 있으며, '샘플 분석'에는 유전체를 분석하는 'WGS(Whole Genome Sequencing)', RNA를 분석하는 'WTS(Whole Transcriptome Sequencing)'을 위해 '차세대 염기서열 분석(NGS: Next Generation Sequencing)', 'PCR(Polymerase Chain Reaction)', '마이크로어레이(Micro Array)', '질량분석법(Mass Spectrometry)' 등의 기법들이 활용되고 있다.
반응형2-1. '순환종양세포'의 분리 기술
일반적으로 종양세포는 기원에 따라 그 특징이 매우 다양하며, 이를 활용하여 연구자들은 '순환종양세포(CTC)'의 분리기술을 개발하였다. 암세포가 혈액 내 백혈구보다 크기가 큰 것을 이용하여 '멤브레인에 걸러서 분리하는 방법', 밀도를 이용한 '피콜 원심분리 방법', '암세포의 전하 차이를 이용하는 방법', '미세유체칩을 이용하는 방법' 등 다양한 원리를 이용하여 순환종양세포를 분리하고 있다. 아래의 표는 '순환종양세포(CTC)'의 '분리방법', '분리기술', '개발 회사'를 정리한 것이다.
분리된 '순환종양세포(CTC)'는 다양한 분석 방법을 통하여 응용된다. '순환종양세포'의 수를 기준으로 암의 진행 상황에 대한 연관성을 분석할 수 있으며, 세포 염색을 통하여 순환종양세포의 형태적인 특징을 분석할 수도 있다. 또한 유전자의 발현을 분석함으로써, 순환종양세포에 특이적으로 발현하는 유전자들을 찾아낼 수 있다.
분리방법 분리기술 회사 면역자기성 분석
Immunomagnetic assays
(EpCAM antibodies)CellSearch 얀센 진단(Janssen Diagnostics) AdnaTest 애드나젠(AdnaGen) Anti-EpCAM / anti-CK antibody CTC enrichment 글렌 덩(Glenn Deng), 스탠포드 대학교(Stanford University) Dynabeads Epithelial Enrich 라이프 테크놀로지스(Life Technologies) 미세유체칩
(Microfluidics chip)OncoCEE 바이오셉트(Biocept) ClearCell FX System 클리어브리지(Clearbridge) Isoflux 플럭시온 바이오시스템즈(Fluxion Biosystems) CTCChip, Hcrringbonc Chip Daniel Habor and Mehmet Toner, Dana-Farber and MGH 크기 ScreenCell 스크린셀(ScreenCell) CellSieve Creatv 마이크로텍(Creatv Microtech) CellOptics 아이코니시스(Ikonysis) 크기 및 변형성 Parsortix 앵글(ANGLE) CleaeCell FX System 클리어브릿지(Clearbridge) 밀도 OncoQuick 그리너 바이오원(Greiner BIoOne) Maintrac SIMFO 2-2. '순환종양세포'를 활용한 임상 연구
'순환종양세포'에 대한 임상 연구는 다양한 '암에 대한 항암제 반응성' 연구에 초점이 맞추어져 있다. 특히 유방암의 항암제 반응성에 대한 연구가 가장 많이 진행되고 있으며, ClinicalTrials.gov의 2020년 기준 180건 이상의 임상연구가 등록된 것으로 확인된다.
- 순환종양세포 '수'를 측정하는 임상 연구: 대표적으로 'CirCE01 임상 연구(NCT01349842)'는 French Multicenter에서 주도하여 유방암 환자에게 항암제를 투여한 후, '혈액 내 순환종양세포 수'를 측정하여 항암제 반응성 여부를 확인하는 것이다. 해당 연구는 '순환종양세포 수의 증감'에 따라 '약물의 반응성' 및 '다른 항암제로의 전환에 필요한 판단 기준'을 연구하는 것이다.
- 순환종양세포 '분자적 표현형'을 측정하는 임상 연구: 'CirCe T-DMI 임상 연구(NCT01975142)'에서는 혈액 내 발견되는 순환종양세포의 '수'가 아닌 '분자적 표현형'을 항암제 처리 기준으로 연구하였다. HER2 유전자의 발현여부에 따라 다른 약물을 처방하였으나, 약물 반응성이 나타나지 않은 것으로 확인된다.
반응형3. 순환종양핵산(cfDNA)
암 환자의 종양으로부터 방출된 Cell free DNA를 '순환종양핵산(cfDNA: circulating free DNA)'라고 하며, 이를 통해 '돌연변이(Mutation)', '미소부수체 변화·전환·삭제', '비정상적인 메틸화' 등의 다양한 특성을 분석하고 종양의 유무와 상태를 추정한다.
'순환종양핵산(cfDNA)'를 이용한 암 진단은 매우 극소량으로 존재하는 순환종양핵산을 활용하여, 환자에게 발생한 돌연변이를 분석해야 하므로 매우 고감도의 유전자 증폭기술이 필요하다. 초기 '시퀀싱(Sequencing)' 기술은 일관성 및 신뢰성의 부족으로 생체지표로 활용하는 데 한계가 있었다. 최근에는 '마그네틱 비드(Magnetic Bead)'를 이용한 BEAMing 기법이나 Digital PCR, TAM-Seq 등의 고감도 분석 기법들이 개발됨에 따라 응용 가능성이 높아지고 있다.
3-1. '순환종양핵산' 분석 기술
암의 경우, 세포의 성장이 비교적 빠르며 '세포사멸(Apoptosis)' 및 '괴사(Necrosis)'가 활발하다. 이러한 과정에서 '순환종양핵산(cfDNA)'은 대식세포에 의해 모두 제거되지 못하고 혈액으로 방출되는 것으로 알려져 있으며, 건강한 사람보다 암 환자의 혈액에서 더 많은 양이 발견된다. 종양에서 특이적으로 발견되는 '순환종양핵산'은 정확한 생물학적인 메커니즘이 검증된 것은 아니지만, 암세포의 사멸과 밀접한 연관성이 있는 것으로 보고되고 있다.
암 진단을 위하여 매우 극소량 혈액 내에 존재하는 '순환종양핵산'을 분리하고, 돌연변이까지 확인하기 위하여 필수적으로 초감도의 유전자 증폭기술이 필요하다. 초기 시퀀싱 기술은 순환종양핵산을 분석하기에는 다소 어려움이 있었으나, 최근 개발된 초감도의 '차세대 염기서열분석(NGS: Next Generation Sequencing)', '디지털 PCR(Digital Polymerase Chain Reaction)', 'BEAMing' 등 다양한 기술이 활용되고 있다.
'순환종양핵산(cfDNA)'은 종양의 크기 및 진행 정도에 따라 혈액으로 유입되는 양이 증가하는 것으로 알려져 있으며, 혈액 내 반감기는 2시간 내외로 매우 짧아 환자의 최신 정보를 제공할 수 있다. 또한 유전적 정보를 확인할 수 있어, 잔존하는 암세포 및 전이 여부 등의 추적 관찰에도 효과적으로 활용될 수 있다. 더불어 '표적치료제 사용을 위한 특정 유전자의 돌연변이 여부 확인', '약제 내성 예측', '후성유전학 등의 분석'에도 활용될 수 있어, 암의 조기진단 및 치료에 매우 유용하게 활용될 수 있다.
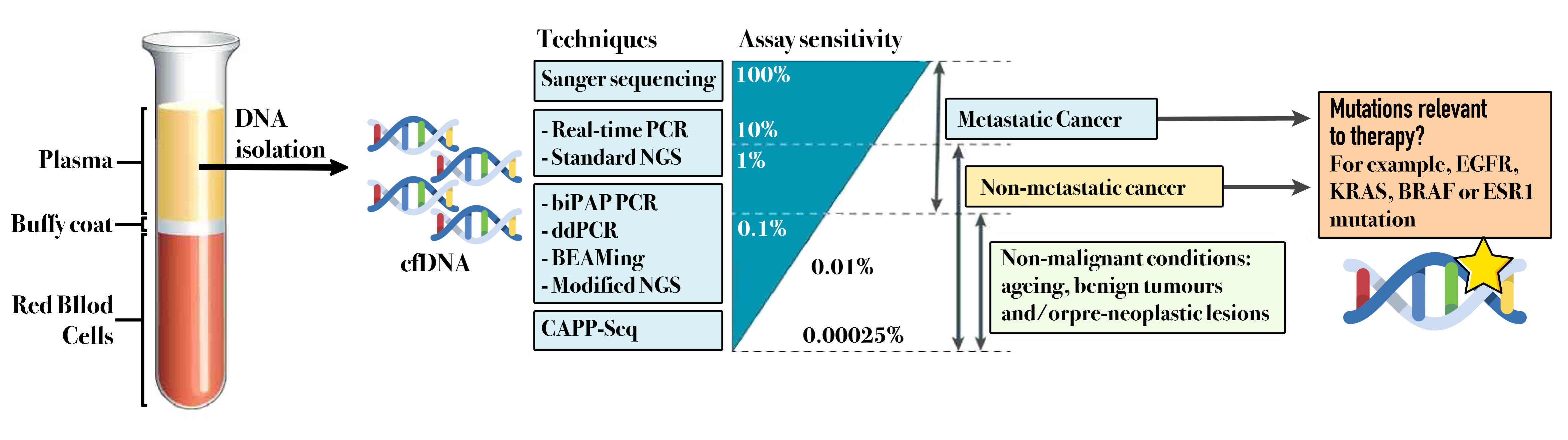
순환종양핵산의 분리 및 분석 기술 / 출처: Nature Review Clinical Oncology(2019) 3-2. '순환종양핵산'을 활용한 임상 연구
액체생검 기반 임상연구 중, '순환종양핵산(cfDNA)' 연구가 가장 활발하게 진행되고 있다. '순환종양핵산' 연구는 주로 '재발 및 전이', '미세 잔존 질환 진단', '조기 진단'으로 구분된다.
- 약물치료의 반응성을 살펴보는 임상 연구: 그 대표적인 예로 'B-FAST 임상연구(NCT03178552)'는 진행성 도는 전이성 비소세포폐암을 대상으로 순환종양핵산에서 암관련 '체세포 돌연변이'(Somatic Mutation)' 또는 '종양 변이 부담(TMB: Tumor Mutational Burden)'에 대한 분석을 기반으로 환자들에게 적용될 치료방법을 제시하기 위한 연구이다. '순환종양핵산(cfDNA)'의 돌연변이 여부에 따라 약물치료의 반응성을 살펴보는 것을 목적으로 임상 연구를 수행하였다.
- 암의 치료 정도를 판단하는 임상 연구: '순환종양핵산(cfDNA)'의 잔존 여부 확인을 통해 암의 치료 정도를 판단하는 임상 연구도 활발하게 진행되고 있다. 'c-TRAK TN 임상 연구(NCT03145961)'는 1차 표준 치료를 받은 Triple-negative 유방암 환자를 대상으로 12개월 내 순환종양핵산에 대해서 양성인 경우, 약물처방군 도는 관찰군으로 나누어 관찰함으로써 '순환종양핵산'의 미세 잔존 여부에 따른 암의 치료 또는 재발 여부를 판단하는 연구를 수행하였다. 즉, '미세잔존질병(MRD: Minimal Residual Disease)' 확인을 위한 순환종양핵산의 활용 연구다.
- 조기암 발견을 위한 임상 연구: 순환종양핵산을 활용하여 조기암 발견을 위한 임상 연구도 진행되었다 대표적으로 SUMMIT 임상 연구(NCT03934866)'는 50~77세 연령의 50000명을 대상으로 흡연을 하는 폐암 발생 고위험군과 저위험군으로 나누어 혈액을 채취하고 '순환종양핵산'을 분석하여 암 발생 초기 단계에 과련된 정보 및 진단 '마커(Marker)'로서의 응용 가능성을 연구하였다.
반응형4. 엑소좀(Exosome)
'엑소좀(Exosome)'은 모든 살아있는 세포에서 발견되는 '미세소포(Microvesicle)'이다. 대부분 '엔도솜 막(Endosomal Membrane)'으로부터 유래되며, 세포 내 소화 작용을 위해 '리소좀(Lysosome)'과 융합되는 대신에 '세포막(Cell Membrane)'과 융합되면서 형성되는 것으로 알려져 있다. 또한 세포에서 방출될 시, 30~150nm 크기의 소포 형태를 가지며 'DNA', 'RNA', '단백질' 등을 포함하고 있는 것이 특징이다. '혈액', '소변', '침', '눈물', '모유' 등에서도 검출되며 일반적으로 세포 간의 신호 전달 등 다양한 기능을 수행하는 것으로 알려져 있어, 질환 상태의 파악 및 치료 평가에 활용될 수 있을 것으로 기대된다.
'엑소좀(Exosome)'은 환자의 혈액으로부터 분석이 가능한 수준으로 충분히 확보될 수 있으나, '초원심분리(Ultracentrifugation)'을 이용한 엑소좀의 분리는 낮은 수득률과 시간적 문제로, 종양으로부터 엑소좀을 선별적으로 분리하는데 어려움이 있다. 이런 한계를 극복하고자 다양한 연구자들은 분리기술을 개발하고 있다. 하지만 현재 표준화된 분리·분석 방법이 존재하지 않아, 실제 현장에서 활용되는데 물리적 시간이 필요할 것으로 예상된다.
4-1. '엑소좀'의 분석 기술
세포들은 주변세포 또는 외부 환경과의 커뮤니케이션을 위하여 중간 매개체로서 다양한 물질들을 외부로 분비한다. 대표적인 매개체는 '사이토카인(Cytokine)', '케모카인(Chemokine)', '호르몬(Hormone)' 등의 있으며, 최근에는 엑소좀을 통한 세포 간 정보교환에 대한 연구가 활발하게 진행되고 있다.
'엑소좀(Exosome)'은 '단백질(Protein)' 및 '핵산(Nucleic Acids)' 등의 유전물질을 포함하고 있으며, 유래된 세포들의 특성 및 상태에 대한 정보를 보유하고 있다. 또한 '혈액', '소변', '침', '눈물', '모유' 등 다양한 체액들은 질병의 상태를 알려주는 주요한 표지자이다. 다른 액체생검 요소보다 상대적으로 매우 높은 농도로 존재하며, 내부 물질들이 질병의 자세한 정보를 제공하고 있어 중요한 '바이오마커(Biomarker)'로 많은 연구가 진행되고 있다. 다만 '엑소좀을 분리하는 방법'이 매우 다양하고 의학적으로 응용하기 위한 표준화가 정립되어 있지 않은 실정이다. 또한 분리법에서 사용되는 시료의 양이 다르며, '회수율', '순도', '소요 시간' 등이 상이하여 지속적인 연구가 필요하다.
'엑소좀(Exosome)'을 이용한 '바이오마커(Biomarker)' 발굴 연구는 엑소좀 내 '마이크로RNA(microRNA)' 분석에 중점을 두고 진행되고 있다. 암 환자들의 혈액 내 엑소좀을 분석하여 microRNA에 대한 '프로파일링(Profiling)'을 수행하여 암 특이적 '바이오마커(Biomarker)'를 발굴하고 있다.
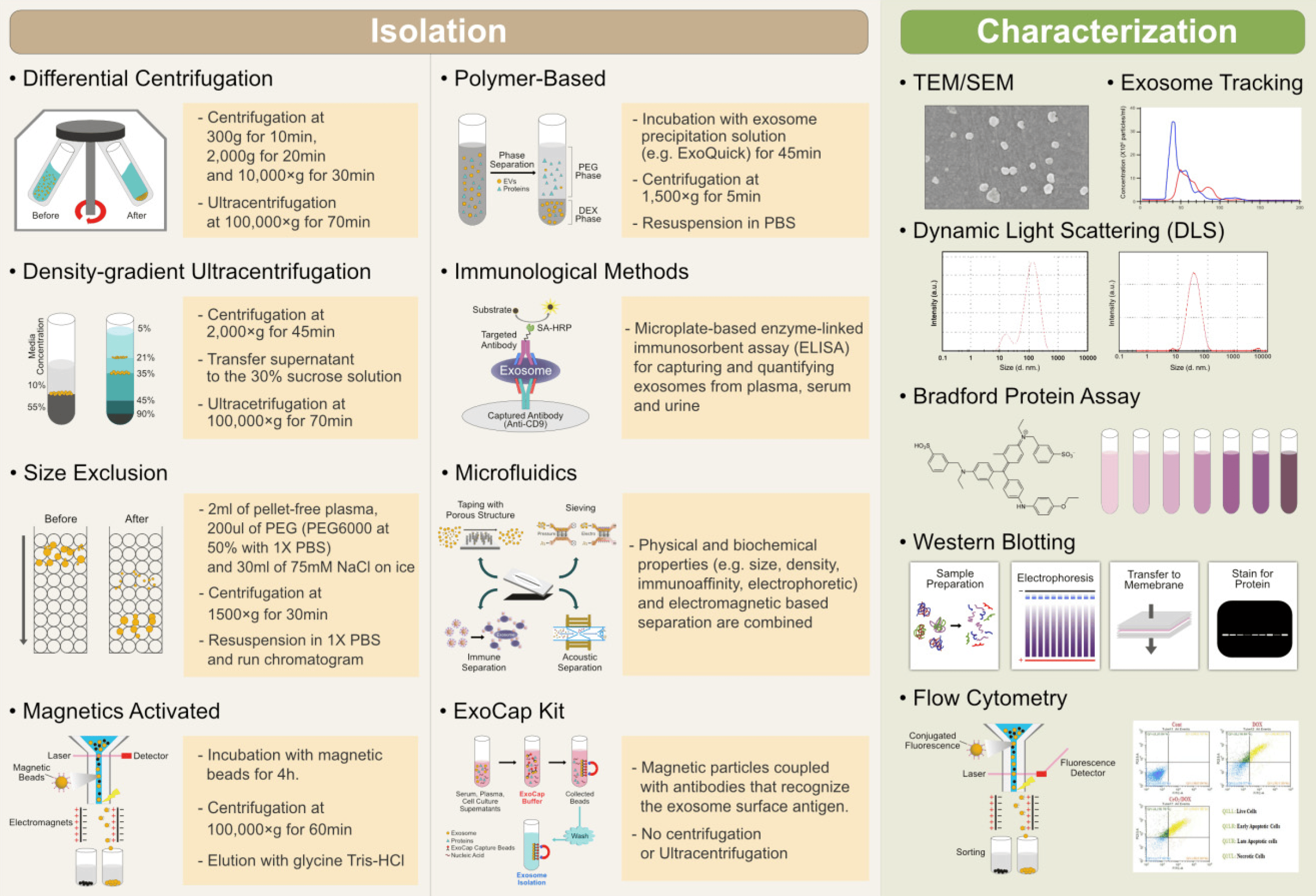
엑소좀의 분리 및 분석 방법 / 출처: Cells(2019) 4-2. 소화기암에 대한 엑소좀 microRNA 분석 연구
'엑소좀(Exosome)'은 암 특이적 '바이오마커(Biomarker)' 발굴을 위해서 엑소좀 내 '마이크로RNA(microRNA)' 분석에 초점을 두고 있다. 대표적인 예로 소화기암 종류에 따라 엑소좀 내 microRNA 발현 패턴을 분석하여 상이한 것을 확인하였다. 아래의 표는 소화기암 종류에 따라 '발현 증가' 또는 '발현 감소'한 mircoRNA 발현 패턴을 표로 정리한 것이다. (출처: Cancer Gene Therapy, 2016) 이렇게 증감한 유전자들에 대한 발현 분석으로 암 환자의 '진단', 진행 상황', '예후' 등을 예측하기 위한 연구가 수행되고 있다.
암종 발현 증가 발현 감소 위암 miR-21, miR-103, miR-223, miR-17/92 miR-34b/c, miR-218, miR-10b, let-7 대장암 miR-1224-5p, miR-1229, miR-1246, miR-150, miR-21, miR-223, miR-23a, miR-19a, miR-17/92 miR-143, let-7, miR-145, miR-195, miR-130a, miR-331, miR-124a, miR-542-3p, miR-34a 췌장암 miR-17-5p, miR-30, miR-92-1, miR-99a/b, miR-100, miR-103, miR-107, miR-125a/b, miR-130a, miR-132, miR-204, miR-211, miR-342, miR-155, miR-15b, miR-95, miR-186, miR-190, miR-196a, miR-200b, miR-211/222, miR-21, miR-125b miR-29c, miR-30a-3p, miR-96, miR-130b, miR-141, miR-148a/b, miR-126, miR-127, miR-375, miR-494, miR-34a 식도암 miR-21, miR-1246, v3202, miR-23a, miR-718, miR-3610, miR-4271, miR-33a, miR-326, miR-16-5p miR-34a, miR-144, miR-106b, miR-486-5p, miR-93, miR-451, miR-324-5p 간암 miR-21 miR-34a, miR-125b 5. '액체생검'을 통해 '정밀 의료'가 가능해진다.
'정밀 의료(Precision Medicine)'란 환자들에 대한 포괄적인 정보를 분석해 비슷한 특성을 보이는 환자들에게 최적화된 방법으로 질병을 예방·진단·치료하는 것이다. 초기에는 환자 정보의 전산화를 통하여 시작되었으며, 인간의 게놈지도가 완성됨에 따라 유전자 검사를 통한 유전자 정보를 기반으로 자리 잡게 되었다. 이러한 '정밀 의료(Precision Medicine)'는 암 때문에 사망하는 사람의 수를 줄이기 위하여 시작되었으며, 차세대 시퀸싱 기술의 발달로 급속하게 발전하였다. 현재도 암으로부터 생존률과 삶의 질을 높이기 위하여 지속적인 기술의 개발이 이루어지고 있다.
암을 조기에 발견하면 생종률이 증가하나, 암세포 또한 면역체계를 속이며 진화를 거듭하고 있다. 현재 암을 조기에 발견하기 위하여 수행하는 선별검사는 '맘모그램(Mammogram)', '변검사', 'CT 촬영', '내시경' 등으로 모두 민감도 및 특이도의 한계점을 가지고 있다. 또한 해당 과정은 '조직생검(Tissue Biopsy)'를 통하여 확증하고 있으나, 이 또한 매우 불편하고 위험한 것이 현실이다. 이러한 위험과 불편함을 극복하기 위하여 고안된 것이 '액체생검(Liquid Biopsy)'이며, 이는 인체에서 유래된 체액의 성분을 분석하는 것이다. '조직생검' 및 '액체생검' 모두 초기에는 PCR 유전자 증폭 기술을 활용하여 유전자 변이 등을 분석하였으나, 신규 변이를 찾을 수 없다는 한계점이 있다.
한편, '차세대 염기서열 분석(NGS: Next Generation Sequencing)' 기술이 개발·보급됨에 따라, '생물정보학(Bioformatics)'과의 접목이 매우 빠르게 진행되었고, 다양한 유전적 변이 및 신규 변이들까지 분석할 수 있게 되었다. 이에 액체생검 기술은 그 전환점을 맞이하였다. 극소량의 체액 내 시료의 분석이 가능해짐에 따라, 개인의 유전정보를 분석할 수 있게 되었고, 암의 조기 발견 및 유전적 변이에 관한 확인이 가능해지게 되었다. 앞으로 액체생검 기술을 통한 진정한 정밀 의료가 가능해질 것으로 전망된다.
또한 '바이오셉트(Biocept)'의 보고서에 따르면, 액체생검 시장은 크게 응용 분야에 따라 '스크리닝(Screening)', '프로파일링(Profiling)', '동반 진단(Companion Diagnostics)', '모니터링(Monitoring)'으로 구분되며, '스크리닝(Screening)'의 비율이 가장 높은 것으로 확인된다. NGS 기술의 발달에 따라 '유전자 스크리닝(Gene Screening)' 및 '프로파일링(Profiling)' 분야가 급속하게 성장하여, 액체생검 시장에서 가장 핵심적인 응용 분야로 자리 잡은 것으로 판단된다.
반응형6. '액체생검' 관련 기업
'액체생검(Liquid Biopsy)' 산업은 다양한 공공 민간 연구기관의 협을 통하여 새로운 개술의 개발 및 '이머징마켓(Emerging Market)'으로 진출하게 되었다. 대표적으로 유럽 13개국에서 33개의 회사와 연구소로 구성된 Cancer-ID가 암 치료와 모니터링에 사용할 목적으로 '순환종양세포(CTC)'와 '순환종양핵산(cfDNA)'를 동정하는 방법을 표준화하였다. 그 외에도 The National Cancer Institute에서 주도하는 Medicine Intiative, 영국의 18개 대학이 연합한 The Early Cancer Detection Consortium, '일루미나(Illumina)'가 포함된 Worldwid Innovative Networking Consortium 등이 있다. 그 후, 개별 기업들의 다양한 기술 및 제품 개발을 통해 지속적으로 진보하고 있다.
6-1. 클리노믹스(Clinomics)
- 국적: 한국
'클리노믹스(Clinomics)'는 '게놈(Genome)' 기반 암·질병 조기진단 선도 기업으로, '액체생검(Liquid Biopsy)' 및 '다중오믹스(Multi-Omics)' 기술을 통한 '암 조기 진단'과 '질병·노화 정복'을 추구하고 있다. '클리노믹스(Clinomics)'는 세계 최고 수준의 게놈 기반 바이오헬스 정보처리 역량을 바탕으로 '혈액에서 CTC 및 cfDNA를 동시 검출하는 기술' 및 '다중 오믹스 분석 기술'을 통해 주기적인 게놈 기반 암 조기진단 서비스를 제공하는 회사이다. 아울러 독보적 게놈 기술을 기반으로 향후 '유전자 가위(Gene Scissor)' 등 '유전자 치료제(Gene Medicine)' 분야를 선도할 수 있는 기술력을 보유한 '바이오테크(Bio-Tech)' 기업이다.
- 액체생검 플랫폼(Liquid Biopsy Platform): '액체생검 플랫폼' 상품은 환자의 '체액(소변, 타액, 주로 혈액)'을 분석하여 혈액 속의 '순환종양세포(CTC: Circulating Tumor Cell)'나 '순환 종양 핵산(cfDNA: cell-free DNA)'을 검출하고 이를 분석하는 기술이다. '클리노믹스'는 국내외 다른 액체생검 회사와 차별화된 기술을 보유하고 있다. 다른 회사는 CTC나 cfDNA 어느 하나에 집중하고 있지만, 클리노믹스는 2020년에 'OPR-2000'이라는 완전 자동화 'CD-PRIME(혈액 원심분리기)'을 개발 완료하여 CTC와 cfDNA를 동시에 검출할 수 있다. 관련된 '클리노믹스(Clinomics)' 제품으로는 'CD-Lbx™1', 'CD-LBx™2', 'CD-FAST™Auto'가 있다.
- 암 진단·모니터링: '암 진단·모니터링' 상품은 암 환자의 조직이나 혈액에서 암을 유발하는 유전자의 변이 상태를 분석하여 암 치료나 처방을 위한 정보를 제공하며, 치료 이후의 변이 상태를 지속적으로 모니터링하는 상품이다. '클리노믹스'가 현재 보유하고 있는 암 진단·모니터링 'Cancer-PRIME', '간암 패널', '부인암 패널'이 있다. '클리노믹스'는 '유전자 진단 패널 제조 기술'을 기반으로, 표적항암제 관련 유전자의 분석뿐만 아니라, 환자의 혈액에서 수득한 cfDNA, CTC를 분석하여 '폐암', '간암', '부인암', '고형암'을 진단 모니터링할 수 있는 유전자 분석 패널을 개발하였다. '동반진단(Companion Diagnosis)' 같은 항암제를 투여해도, 어떤 환자는 암이 완전히 없어지고 다른 환자에게는 효과가 전혀 없거나 저항이 생기는데, 이는 환자의 유전적 특성 및 변이에 따른 개인의 차이에 기인한다. 즉 '동반진단(Companion Diagnosis)'이란 이러한 개인별 유전 특성 및 변이를 진단하고, 의약품을 선택 치료하는 것을 의미한다. 의약품의 반응률을 높이고 부작용을 최소화하여 환자의 삶의 질을 향상시키며, 불필요한 처방을 줄여 의료비를 절감하고, 보험 재정 건전화에 기여하는 등 동반진단은 개인 맞춤형 의료의 근간이 되고 있다. '클리노믹스'는 '비소세포폐암 동반진단 키트(ROS1 유전자 Fusion 검사)' 등을 통하여, 비소세포성 폐암의 ROS1 유전자 Fusion 여부를 특이적이고 민감하게 검출해 내는 등 다양한 동반진단 서비스를 수행 중이다. 현재 출시하고 있는 서비스로는 'ROS1(비소세포성 폐암)', 'PIK3CA(유방암)', 'KRAS(폐암, 대장암)' 등이 있다.
- '다중오믹스(Multi-Omics)' 기반 조기진단: '다중오믹스(Multi-Omics)' 기반의 조기진단 상품은 혈액 등으로부터 개인의 '유전체(Genome)' 정보는 물론 '외유전체(Epigenome)', '단백질체(Proteomics)', '발현체(Expressionmics)', '대사체(Metabolomics)' 등 정보를 종합하여 질병의 가능성을 예측 또는 조기진단하는 상품이다. 클리노믹스가 개발 중이 질병 조기진단 상품으로는 '우울증(Stressomics)', '심근경색(Cardiomics)' 등이 있고, 암 조기진단 상품으로는 '대장암', '폐암', '위암'등의 상품이 있다. '암 조기진단(폐암, 위암, 대장암)'은 기존에 잘 알려진 '단일염기다형성(SNP)', '체세포 돌연변이(Somatic Muation)' 기반의 연구결과의 한계점을 극복하고, 다양한 암종에 대한 특성에 따라 정확한 진단 예측이 가능하도록 하기 위해서는 '외유전체(Epegenome)' 분석이 필요하다. 위의 다중오믹스 데이터 분석은 '오믹스별·오믹스간 암 영향력·상관성'을 밝히는데 유용하다. 또한 암 조기 진단에 필요한 가장 정확한 '바이오 마커(Bio Marker)'의 발굴을 가능하게 한다. 또한 '클리노믹스'는 '혈액', '위액' 등을 이용한 비침습적인 '액체생검'을 기반으로 분석·검사를 진행하기 때문에 '암 조기 예측', '조기진단' 등 실질적인 다양한 기술 구현이 가능하다.
- 바이오 빅데이터 센터(BBC: Bio Big data Center): 폭증하는 바이오 및 의료 데이터를 표준화하고 분석·처리·저장하기 위해 대용량 전산 하드웨어 기반 게놈·건강·의료 정보 '클라우드(Cloud)' 상용화의 필요성은 더욱 강하게 대두되고 있다. 수십·수백 테라바이트 이상의 '게놈 데이터(Genome Data)'를 국내·외 간 네트워크로 빠르게 전송하기 위한 '초고속 전송 기술'과 '복잡한 프로그램', 'DB를 효율적으로 처리·관리해 주는 서비스'는 '빅데이터(Big Data)' 분야에서 필수적인 요소이다. 융합시대의 도래에 따라 '바이오 정보', '건강 정보', '의료 정보'의 통합적 '빅데이터 분석(Big Data Analysis)' 및 '데이터 배포'의 필요성이 높아짐에 따라, '클리노믹스'는 자체적인 '바이오 빅데이터 센터(BBC: Bio Big data Center)' 구축을 통하여 이러한 시대적 흐름에 발 빠르게 대처해 나가고 있다.
6-2. 마크로젠(Macrogen)
- 국적: 한국
'마크로젠(Macrogen)'은 1997년에 설립된 업체로, '유전체 분석 서비스', '올리고 합성', '마이크로어레이 분석 서비스', '유전자 편집 마우스', '임상진단 서비스', '개인유전체 분석 서비스' 등의 사업을 영위하고 있다. 유전자 정보를 빠르게 읽어내는 기술인 '차세대 염기서열분석(NGS: Next Generation Sequencing)' 기반의 진단 기술을 보유하고 있다.
6-3. EDGC(이원다이애그노믹스)
- 국적: 한국
'EDGC(이원다이애그노믹스)'는 2013년에 설립된 업체로, '의원 의료재단'과 'DIAGNOMICS'사가 함께 인천 송도 경제 자유구역에 설립한 한미합작 법인이다. 'EDGC'는 '유전자 분석 진단', '체외 진단(In-vitro Diagnostics)' 시장의 '암 조기진단'을 주사업으로 영위하고 있으며, 국내외 비즈니스 네트워크를 기반으로 사업화를 이끌고 있다. EDGC는 cfDNA 액체생검 기술을 기반으로 '폐암 조기진단 액체생검인 'EDGC S-CAN™'을 상용화하였고, 임산부의 혈액을 이용한 태아의 염색체 이상 진단 검사인 '태아 DNA 선별 검사(NIPT: Non-Invasive Prenatal Test)'를 개발하여, 싱가포르·태국·필리핀 등지로 수출하였다. 또한 '마이크로어레이 플랫폼 기반 유전체 분석 상품인 '신생아 유전자 검사 베베진', '개인 헬스케어 서비스 진투미', '유전성 안과질환 예측검사 마이아이진' 등을 보유하고 있다. 또한 '유전체 빅데이터(Genomic Big Data)'를 자체적으로 구축하고 있어 한 번의 유전자 검사로 다양한 질환 검사 서비스를 제공할 수 있는 기술을 확보하고 있다.
6-4. 지노믹트리(Genomictree)
- 국적: 한국
'지노믹트리(Genomictree)'는 2000년에 설립된 업체로, '체외진단(In-vitro Diagnostics)' 시장의 '암 조기진단'을 주력산업으로 영위하고 있다. 보건의료 시장 요구를 충족시키기 위하여 특정 암을 조기에 진단할 수 있는 '고성능 신규 DNA 메틸화 바이오마커'를 이용한 체액 기반 비침습적 암 조기진단 기술 개발에 주력하고 있다. 특히, 대장암 환자의 혈액에서 유리된 DNA를 찾아 정량적 유전자 증폭 방법인 LTED-qMSP assay를 적용하여 Syndecan-2 유전자의 '메틸화(Methylation)' 정도를 산출하는 기술을 보유하고 있다. 혈액검사를 통해 대장암을 조기진단할 수 있는 EarlyTect-GI SDC2 Kit을 생산하여 2014년에 식약처로부터 품목허가를 받았다.
6-5. 파나진(PANAGENE)
- 국적: 한국
'파나진(PANAGENE)'은 2001년에 설립된 업체로, 'PNA 유전자 진단 제품' 개발·제조·판매에 관한 사업을 영위하고 있다. '당(Sugar)'과 '인산기(Phosphate Group)'로 이뤄진 유전자 골격을 '펩타이드(Peptide)'로 바꾼 인공 유전자인 '펩토오스핵산(PNA: Perptide Nucleic Acid)'을 이용한 RT-PCR clamping 기술로, 2012년에는 '세계 일류상품', 2013년에는 '대한민국 10대 기술대상'을 수상했다. 이 기술을 바탕으로 암 조직세포에서 표적항암제 처방 기준이 되는 유전자 돌연변이 발생 여부를 검사하는 진단 기술을 개발하고 있다.
6-6. 일루미나(Illumina)
- 국적: 미국
'일루미나(Illumina)'는 유전체 염기서열 분석기업으로, '마이크로어레이(Micro Arrays)', '차세대 염기서열분석(NGS: Next Generation Sequencing)' 장비와 소모품 시장을 주도하는 업체 중 하나이다. 한편, '일루미나(Illumina)'의 계열사인 '그레일(Grail)'은 cfDNA 검출을 위해 Ultra-deep sequencing 기술을 이용하고 DNA 분석비용을 낮추는 연구를 진행 중이다.
반응형6-7. 그 외 기업
기업명 개발·사업화 ANGLE PLC - Microfluidics 기법으로 CTCs를 포집하는 'Parsortix 기술'로 CE 인증을 받고 FDA 승인을 받음. FLUXION BIOSCIENCES INC. - CTCs를 분리하는 IsoFlux System을 상용화함. Thermo Fisher Scientific - Ion Torrent System은 DNA-Sequencing 적용을 위해 센서를 통한 전기·이온의 변화를 검출하는 장비로 다양한 액체생검법에 활용됨 . Qiagen - 엑소좀으로부터 RNA를 정제하는 키트를 개발함.
- Cell Microsystems사의 Single Cell 분리 기술을 도입함.
- Therascreen EGFR RGQ Plasma PCR kit로 CE-IVD 마크를 받음.Biocept - General Electric사에서 설립한 액체 생체검사 업체임.
- EGFR 돌연변이를 분석하여 비소세포성폐암을 진단하는 기기를 상품화함.
- CLIA-certified Laboratory를 운영하여 암환자의 혈액으로부터 microfluidics 기반으로 CTC를 분리하고 cfDNA 분석을 서비스함.Bio-Rad - GnoBio로부터 droplet-based sequencing technologies를 획득하여 임상진단 시장에 진출함. Cynvenio - CTC와 cfDNA를 동시에 검출하고 분석하여 진단함.
- microfluidic chip 상에서 항체기반으로 자동화된 CTC 샘플준비와 유전자 분석 및 이미징을 진행함.Exsome Diagnostics - Biofluid 기반으로 한 circulating exosomal RNA와 cfDNA 진단기술을 개발하고 상업화함. Trovagene - Sequenom으로부터 urine-based prenatal testing 권리를 받음.
- 독자적인 DNA 농축기술을 이용해 소변 내의 유전자 분석과 암 진단 시장에 진입함.Genomic Health - RT-PCR을 기반으로 한 진단법을 개발함.
- 방광암에서 사용될 수 있는 cfDNA 검진법을 개발함.Sysmex Inostics - 머크와 OncoBEAM RAS CRC 방법을 공동 개발하여 CE 인증을 받고 상업화함.
- 기존의 조직 기반 검사와 동일한 효과가 확인됐으며, '얼비툭스'와 같은 항 EGFR 치료가 적합한 환자 판별에 사용함.Roche - 세계 체외진단 시장의 리더업체임.
- 유전자 분석장비 시장에서 '일루미나(Illumina)', 'Lfe Technologies, PacBio와 경쟁함.
- 비소세포폐암 표적치료제인 Tarceva의 처방을 위한 동반진단용으로 cobas EGFR Mutation Test V2를 FDA로부터 승인받음.싸이토젠 - CTC 검출 및 분석 기술을 개발함.